
前言:随着多组学联用技术的兴起,传统单一技术越来越难以满足单细胞维度的高通量实验需求。FISH-Flow技术整合了荧光原位杂交(FISH)与流式细胞术(Flow Cytometry,FC)不止能替代抗体完成目标检测,更能在单细胞分辨率下,同时实现转录组(特定RNA)与蛋白质组(表面/胞内标志物)的高通量定量分析,为流式细胞术拓展了全新的检测维度,我们称之为“双面验钞机”。
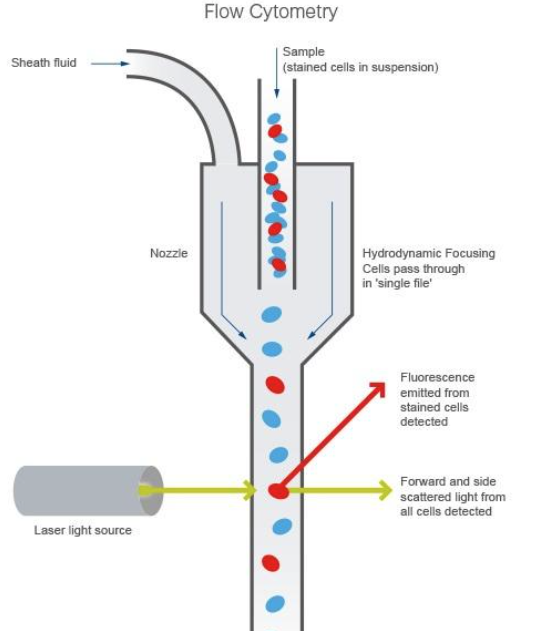
流式细胞术(Flow Cytometry,FC)是一种在液流系统中,快速测定单个细胞或细胞器的生物学性质,并把特定的细胞或细胞器从群体中加以分类统计或收集的技术。其特点是通过快速测定库尔特电阻、荧光、光散射和光吸收来定量测定细胞 DNA含量、细胞体积、蛋白质含量、酶活性、细胞膜受体和表面抗原等参数,并能根据这些参数将不同性质的细胞分开,以进行分析和分选。
荧光原位杂交(FISH)是将被标记的核酸探针与待测样本中的核酸序列按照碱基互补配对的原则进行杂交,经过放大系统进行显色后直接在荧光显微镜下观察的技术。
而整合了以上技术优势的FISH-Flow技术不仅打破了传统流式细胞术依赖抗体的局限,更攻克了FISH技术在单细胞层面难以实现高通量定量分析的不足,从而将二者的优势深度融合,它实现了在单细胞分辨率下,对特定RNA转录本和蛋白质标志物的同步、高通量检测,为多维度的组学分析提供了全新的技术路径。
FISH-Flow的本质是在单细胞精度上实现“看得见”与“数得清”的整合,并在RNA和蛋白两个维度上建立关联。基于这一技术定位,其典型应用场景可归纳为以下5类:
·无抗体可用或现有抗体不合适
基于抗体的流式细胞术实验中,抗体是实验的关键所在,但是很多情况下会面临无合适抗体可用的困境,如:检测不稳定,易内化或快速周转的蛋白、靶向无优质抗体的或全新的抗原、区分高度同源的剪接变体或等位基因、检测“正在合成”而非“已经储存”的蛋白(如分泌蛋白)等。在这些情况下,检测其mRNA是更稳定、更直接或唯一可行的选择,以探针替代抗体,不仅绕开了上述瓶颈,更以制备周期短、特异性强、灵敏度高的优势,让原本“测不了”的样本变得可及。
·检测细胞的“分泌潜能”,直接关联分泌能力与细胞类群
传统的分泌蛋白检测方法(如ELISpot、胞内因子染色),往往需要体外刺激才能捕获蛋白信号,但这会改变细胞原本的生理状态。而FISH-Flow的方法则不同:通过检测特定mRNA,可以在未经刺激、保持原态的细胞中,直接判断其是否在积极准备分泌特定蛋白。例如,从患者样本中直接鉴定出抗原特异性T细胞克隆——只需看其是否携带分泌IFN-γ, TNF-α, IL-2等的mRNA,并同步分析其耗竭标志物(PD-1, Tim-3) 和记忆亚型(CD45RA, CCR7),直接关联免疫细胞的功能输出(cytokine mRNA)、抑制状态(蛋白) 和分化阶段(蛋白),真实还原细胞在体内的功能状态。
·灵敏捕捉病毒RNA的携带细胞:
在浩瀚细胞海中,高效找出极少数携带特定病毒RNA的免疫细胞(如EBV感染),并明确其免疫表型,以探究病毒与宿主的互作机制。
·原位关联微生物物种与功能
在复杂环境样本中,用16S/23S rRNA靶向的FISH探针鉴定特定菌种,同时用抗体检测其保守的代谢酶,实现“谁(物种)-在干什么(功能)”的原位关联。
·追踪肿瘤细胞与耐药机制
在循环肿瘤细胞(CTC) 或患者来源异种移植(PDX)模型中,同步检测上皮-间质转化(EMT)相关转录本(如ZEB1, Vimentin mRNA) 与表面蛋白标志(EpCAM, CD44),揭示转移潜能的动态变化。
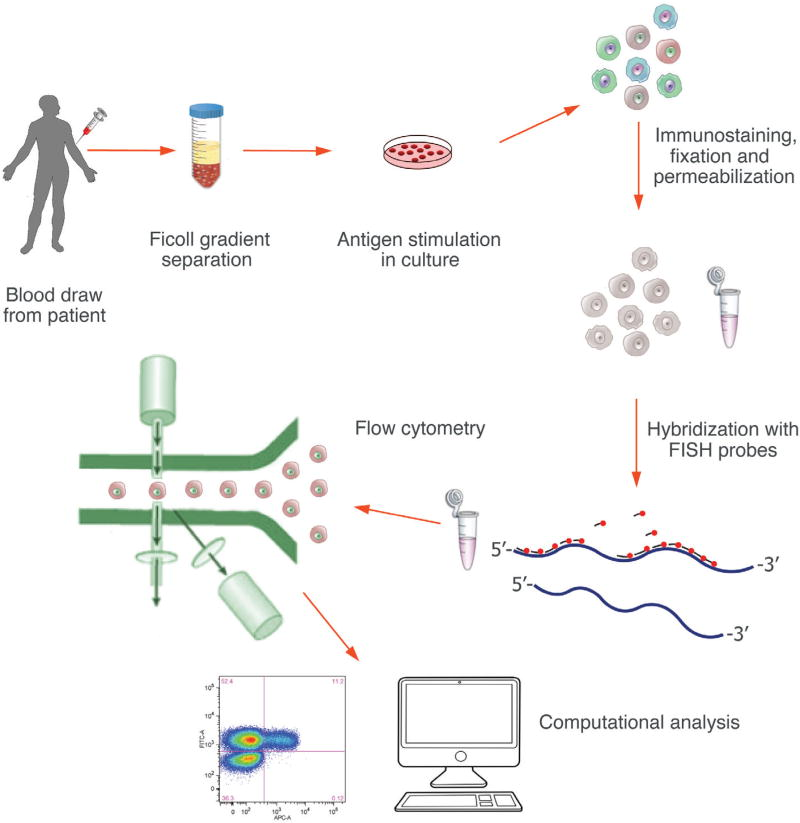
Radford F et, al. Crit Rev Immunol. 2016.
当您的研究满足以下任一条件时,FISH-Flow或应成为比传统抗体流式更优先的考虑选项:
·靶标不稳定:关注的靶点蛋白半衰期极短,或受刺激后迅速变化。
·抗体不可用/不可靠:没有商业化抗体,或现有抗体特异性差、交叉反应高。
·需要核酸层级信息:检测需求为基因融合、点突变、剪接变体或病毒核酸序列。
·避免细胞扰动:希望在不干扰细胞正常生理状态的情况下,研究细胞的实时转录功能状态。
·关联基因表达:需要在同一细胞上将特定的基因表达事件(mRNA)与复杂的免疫表型(多个蛋白标志物)直接关联。
FISH-Flow是在抗体流式方法学存在固有局限性的特定痛点问题上,提供一种基于核酸的、强有力的补充或替代解决方案。它扩展了流式细胞术的检测维度,使其从“蛋白质组”延伸至“核酸-蛋白质组”关联分析,为免疫学、肿瘤学、传染病学研究提供了更精准的工具。如果您的研究靶点符合上述场景,那么FISH-Flow将是比抗体流式更优、有时甚至是唯一的选择。
FISH-Flow并非FISH与流式细胞术的简单叠加,而是为流式技术赋予了RNA层面的检测维度。它直面抗体无法触及的检测盲区,在保持细胞原态的同时,实现了“蛋白表型”与“RNA检测”的单细胞同步解析,这台“双面验钞机”为单细胞多组学研究提供了更可及的技术路径。
Arrigucci R, et al., FISH-Flow, a protocol for the concurrent detection of mRNA and protein in single cells using fluorescence in situ hybridization and flow cytometry. Nat Protoc. 2017.
Vazquez Bucheli JE, et al., Use of FISH-FLOW as a Method for the Identification and Quantification of Bacterial Populations. Mol Nutr Food Res. 2025.
Radford F, et al., Flow Cytometric Characterization of Antigen-Specific T Cells Based on RNA and Its Advantages in Detecting Infections and Immunological Disorders. Crit Rev Immunol. 2016.
Freen-van Heeren JJ. Flow-FISH as a Tool for Studying Bacteria, Fungi and Viruses. BioTech (Basel). 2021.
Ulas M, et al., FISH-Flow Cytometry Reveals Microbiome-Wide Changes in Post-Translational Modification and Altered Microbial Abundance Among Children with Inflammatory Bowel Disease. Pathogens. 2024.