
近日,中国科学院上海营养与健康研究所张亮研究组联合上海交通大学附属第九人民医院李青峰/刘蔡钺教授团队、欧莱雅中国研发和创新中心前沿研究部门黄楠博士团队,在《Journal of Investigative Dermatology》杂志在线发表了题为《High-Resolution Spatial Transcriptomics Unveils Spatially Resolved Gene Modules and Fatty Acid Metabolism Dysregulation in Human Skin Aging》的合作研究成果, 研究利用空间转录组学技术绘制了人类眼睑皮肤衰老的空间图谱,识别出8个空间簇和18个空间基因模块,发现衰老皮肤中皮脂腺脂肪酸合成基因(如FASN、FDPS)显著下调,且表皮中转录因子c-FOS大幅降低;功能实验证实抑制FASN或FDPS可直接导致角质形成细胞衰老和表皮屏障障碍。其中本研究中运用了鲲羽生物自主开发的基于成像的高分辨率空间多组技术(MiP-seq),从组织原位空间维度验证了关键模块基因(如FADS2、APOC1、FLG等)的表达模式。

皮肤衰老涉及转录因子、代谢通路等多维度基因调控网络的失调,如AP-1 家族(如c-FOS)对代谢通路的调控、脂肪酸合成相关基因的表达变化等,但现有研究缺乏空间维度的基因模块互作解析。眼睑皮肤薄且衰老表现显著,同时具备完整皮肤结构,是研究皮肤衰老的理想模型。
研究首先利用空间转录组数据和已有文章发表的单细胞转录组数据,识别出8个空间转录组簇和18个空间共表达基因模块,发现衰老皮肤不仅表现为真皮萎缩、慢性炎症和表皮-真皮通讯减弱,还伴随着皮脂腺中脂肪酸合成关键基因(如FASN、FDPS、ELOVL3等)的显著下调,以及炎症相关基因(如S100A家族)的上调。功能性实验(原代角质形成细胞和3D皮肤模型)证实,抑制FASN或FDPS会显著降低角质形成细胞增殖、诱导细胞衰老,并导致表皮萎缩和屏障功能障碍。此外,转录调控网络分析(SCENIC)发现,衰老表皮中AP-1家族转录因子c-FOS)的表达大幅降低。
以上发现虽能揭示基因表达的空间异质性,但由于Stereo-seq技术本身存在分辨率限制和低表达基因检测灵敏度的局限,因此需要高分辨率的靶向空间组技术来确认关键模块基因的真实表达定位。
研究团队通过高灵敏、高空间分辨率的靶向空间组技术(MiP-seq)进一步验证了40个关键模块基因(如FADS2、APOC1、FLG等)的表达变化,在组织的原位水平证实了空间基因模块的真实存在与组织特异性分布。同时意外发现了全新的、具有组织特异性表达的功能候选基因:GAL(甘丙肽前体),为皮肤功能研究增添了新候选基因,拓展了机制研究方向,也弥补了基于捕获测序空间组技术平台的检测局限。
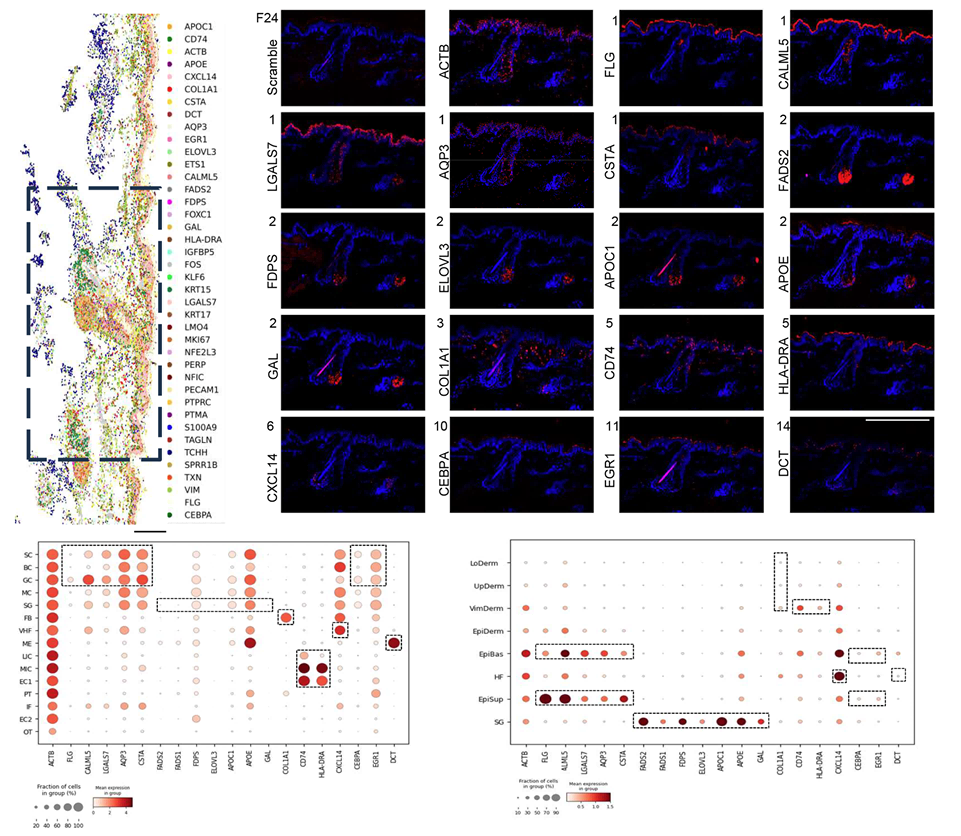
尤其对于表皮角质层的终末分化基因(如 FLG、LGALS7 等),基于原位成像的空间组与基于捕获测序的空间组检测到的衰老相关变化存在差异,原因是角质层中死细胞的致密压缩结构,影响了基于捕获测序的空间转录组技术对于转录本的精准定量。在此研究中基于成像的靶向空间组展示了其在原位检测中的独特优势,使“脂肪酸代谢失调和c-FOS下调驱动皮肤衰老”的核心结论具备了高精度、位置明确的图谱证据。
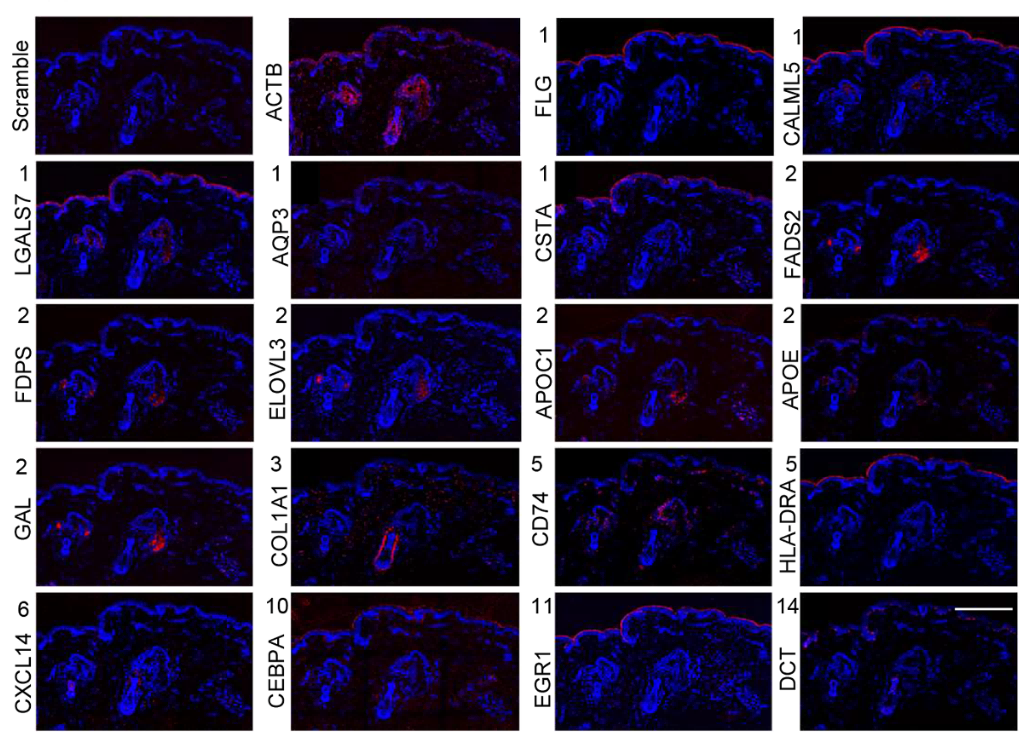

该研究利用单细胞测序与空间组技术绘制了人类皮肤衰老下的高分辨率单细胞空间分子图谱,突破了传统研究在细胞分辨率与空间分辨率的瓶颈,完成了从分子到细胞再到空间位置信息的整合与串联。其发现的FASN/FDPS 脂肪酸合成通路与c-FOS 转录因子,有望成为皮肤抗衰老研究的全新靶点,为衰老机制的研究与抗衰护肤品与药物的开发提供了新的视角与精准的分子图谱。
鲲羽生物自主研发的空间多组学技术(MiP-seq)技术不仅可运用于单细胞精度空间组学图谱构建,同时可实现多层次生物分子(DNA/RNA/Protein)空间分布的验证。其具有灵敏度高、特异性强、可多重检测以及靶标灵活定制、兼容多种物种组织类型等技术特色,为神经生物学、发育生物学、肿瘤研究等领域研究提供更加灵活、多用的工具。
关于此文章的更多精彩研究内容,可以查阅原文进一步探索。
文章原文链接:https://www.sciencedirect.com/science/article/abs/pii/S0022202X25023528
