
在生命科学和临床诊断中,关于基因与蛋白这两个从遗传到功能之间的关系常有一个核心困惑:一个异常的基因片段,是否真的直接会导致异常蛋白生成,亦或是异常蛋白的存在,是不是由于底层基因发生了数量或结构变异?传统的分子检测技术往往将组织打碎提取核酸或蛋白,虽能定量,却丢失了宝贵的空间位置信息与单细胞精度。而传统的DNA FISH与免疫荧光(IF)可以分别实现对基因片段与蛋白的精准定位分析,如果能将两种技术进行高效的结合,便能同一张细胞或组织切片上,同步呈现DNA与蛋白质的原位面貌,便可对基因水平和蛋白水平进行跨组学分析,进一步描述从遗传到功能的关系
在此小编对关于DNA与蛋白共标技术从原理到流程再到应用等方面进行初步的介绍,为大家后面对此技术的选择与使用提供一些参考。
技术本质上是在同一张组织切片或细胞上进行免疫荧光染色和荧光原位杂交反应,实现对特定蛋白质和特定DNA序列(如扩增、缺失、重排)的空间共分布分析。研究者可以通过其直观的结果在单个细胞水平上直接回答:基因的变化与蛋白的存在,进一步辅助细胞类型的鉴定与疾病的诊断。
流程主要参考免疫组化与原位杂交,其中共标的难点在于,DNA杂交所需的通透流程与高温变性条件极易破坏脆弱的蛋白质抗原。因此,流程的设计与实验条件需兼顾两者的完整性。目前主要流程如下:
(1)样本前处理:组织样本通常经过脱蜡、水化,再进行抗原修复和通透处理,以在暴露核酸靶点的同时,尽可能地保持蛋白质抗原的完整性。
(2)免疫荧光先行:通常优先进行免疫荧光染色。一抗结合目标蛋白,二抗携带荧光素(如FITC、Cy3)检测和信号放大。完成染色后,需用交联剂(如多聚甲醛)对样本进行二次固定,以加固抗体与蛋白的结合,抵御后续FISH步骤的冲击。
(3)DNA FISH压轴:通过温度与变性剂使双链DNA解旋变性,随后加入荧光标记的核酸探针与靶序列杂交。洗去非特异结合后,用DAPI复染细胞核。(如需再检测RNA靶标,可以尝试再DNAFISH流程结束后再引入RNAFISH流程)
(4)多通道成像:利用荧光显微镜分通道采集信号,经软件叠加分析,即可直观呈现DNA与蛋白的空间分布。
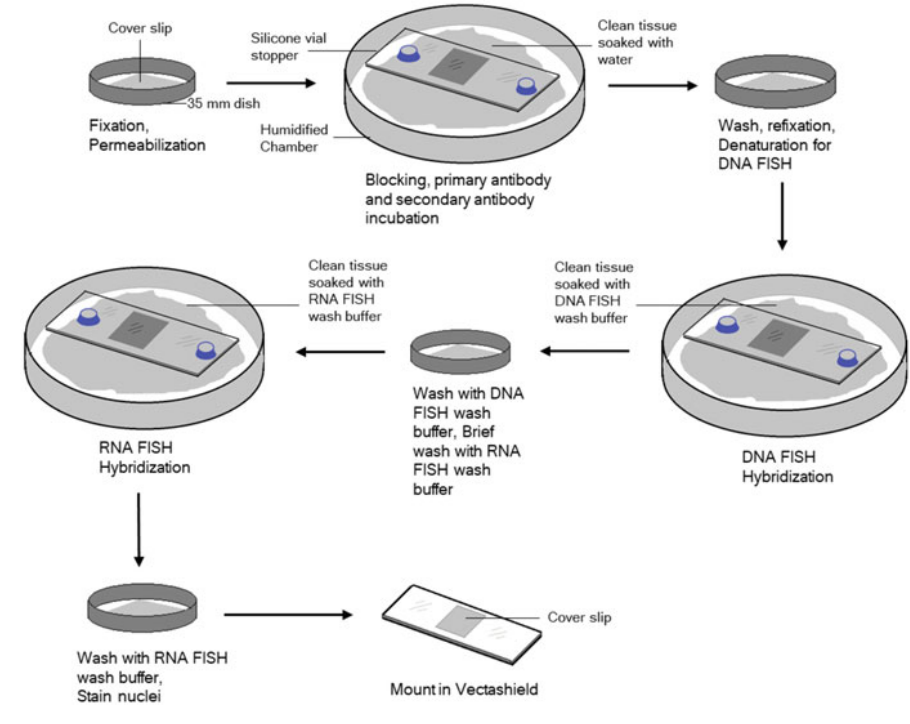
图1 共标流程示意图
共标技术的独特之处在于,将“基因型”和“表型”真正在同一个细胞里对上了号,为肿瘤异质性研究和精准用药提供了关键依据。
乳腺癌HER2精准判读:在乳腺癌诊疗中,HER2蛋白过表达与HER2基因扩增并非总是完全一致。Nguyen等人开发了一种基于微流控和图像处理的高通量方法,发现即使是HER2阳性肿瘤内部,也存在基因扩增但蛋白不表达、或蛋白高表达但基因无扩增的细胞亚群。这种空间异质性直接解释了部分患者对赫赛汀靶向治疗原发或继发耐药的原因,为用药决策提供了双重保险。
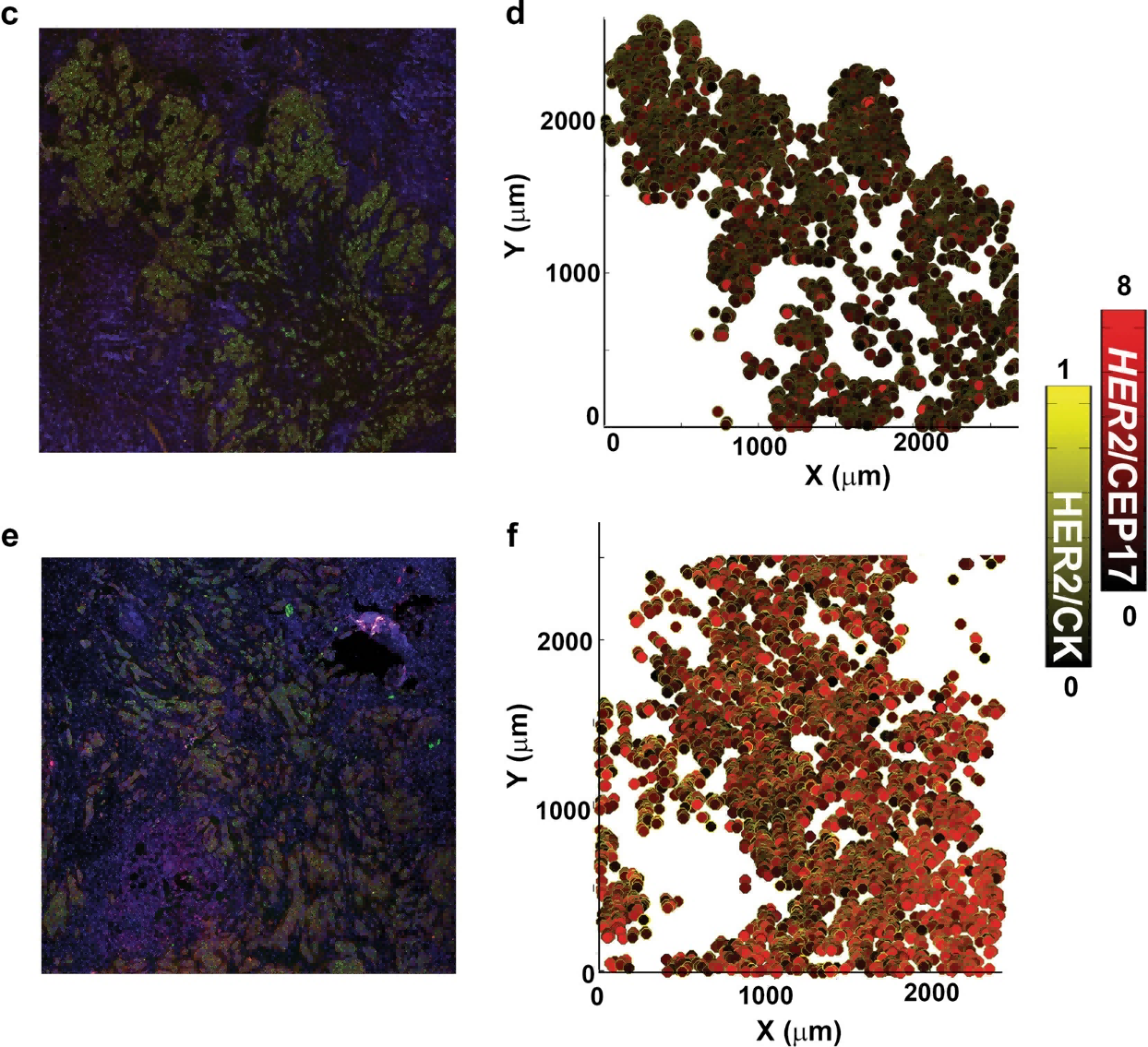
图2:IF-FISH分析细胞系和组织中的HER2评估。
淋巴瘤的“双重打击”锁定:在侵袭性淋巴瘤诊断中,临床需明确MYC基因易位是否与BCL2蛋白高表达发生在同一肿瘤性B细胞中。借助共标技术,病理医生能精准定位出携带融合基因且同时高表达特定蛋白的“双重打击”细胞群,这对明确高侵袭性亚型、指导强化治疗至关重要。
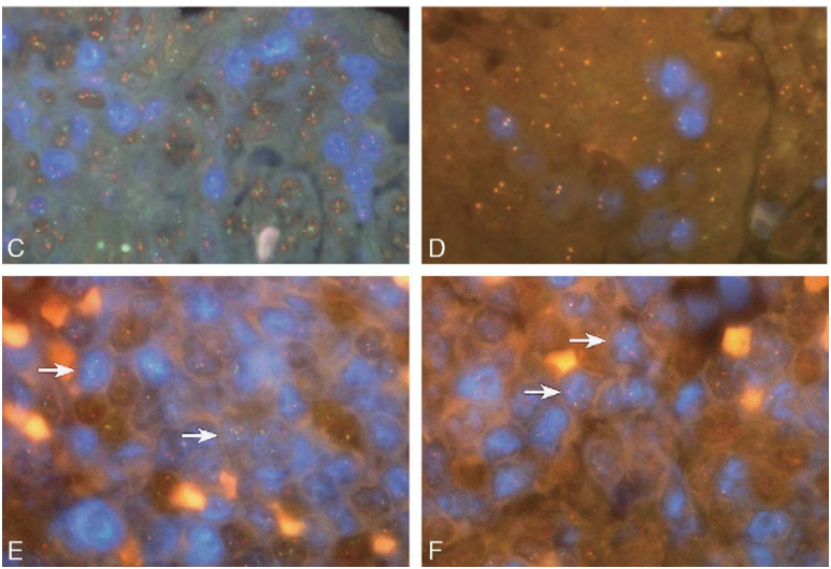
图3:F-TSA 技术应用:免疫表型标记蛋白 cyclin D1 与 IgH/CCND1 双融合易位探针(C、E)或 CCND1 断裂探针(D、F)之间的共表达
宫颈癌筛查的辅助利器:有研究将p16/Ki67蛋白免疫染色与染色体着丝粒FISH探针相结合(iFISH技术),应用于宫颈涂片检测。结果发现,出现染色体非整倍体的细胞数量与病变严重程度呈正相关。该方法在识别高级别癌前病变时展现出高特异性,有望成为传统细胞学筛查的有力补充。
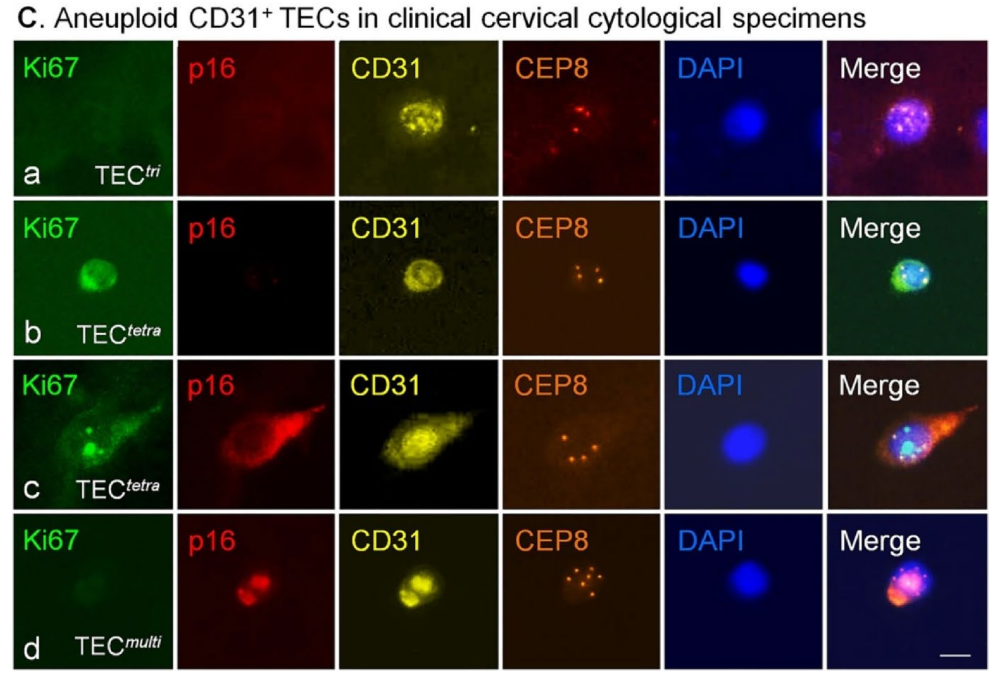
图4:通过宫颈涂片样本检测的非整倍体 CD31*TECs 的代表性图像。
尽管目前该技术流程相对复杂、对操作精度要求高,但随着多重荧光标记技术和人工智能辅助图像分析的发展,共标检测正迈向高通量与自动化。它通过将基因与蛋白信息编织在同一张“细胞地图”上,正默默推动着肿瘤精准诊疗向更微观、更立体的维度迈进。
4 参考文献
1. Sen, Souvik et al. “Combined 3D DNA FISH, Single-Molecule RNA FISH, and Immunofluorescence.” Methods in molecular biology (Clifton, N.J.) ,2024.
2. Nguyen, H. T.,et al., High-content, cell-by-cell assessment of HER2 overexpression and amplification: a tool for intratumoral heterogeneity detection in breast cancer. Laboratory Investigation, 2019.
3. Bzorek, M., et al., Simultaneous phenotyping and genotyping (FICTION-methodology) on paraffin sections and cytologic specimens: a comparison of 2 different protocols. Applied Immunohistochemistry & Molecular Morphology, 2008.
4. Wang, Y. et al. , In situ phenotypic and karyotypic co-detection of aneuploid TCs and TECs in cytological specimens with abnormal cervical screening results. BMC Cancer, 2025.